这一家族中的NRAS、HRAS和KRAS突变引起的癌症占所有人类癌症的近四分之一,使其成为与癌症相关的最常见基因突变之一,几乎覆盖了所有的癌症类型,每年在全球造成100万人死亡。其中,KRAS是最常见的致癌基因(占所有RAS突变的85%),存在于90%的胰腺癌中,30%~40%的结肠癌中,15%~20%的肺癌中(大多为非小细胞肺癌)。

图1. RAS通路调控示意图[1]
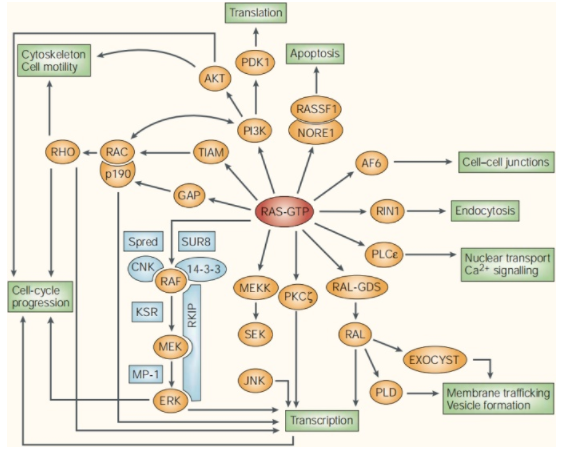
图2. RAS效应物及其生物学响应[1]
KRAS基因最常发生突变的位点是第 12、13和61位密码子。在所有的突变类型中最常见的7个突变热点为:G12C、G12S、G12R、G12V、G12D、G12A、G13D,其中G12突变常导致G12C、G12V或G12D替换,分别占NSCLC中KRAS突变的40%、19%和15%。

图3. 选择性KRAS-G12C抑制剂的发现[2]

图4. RAS信号通路及相应肿瘤治疗策略[3]

图5. Sotorasib 3 期临床试验结果[4]
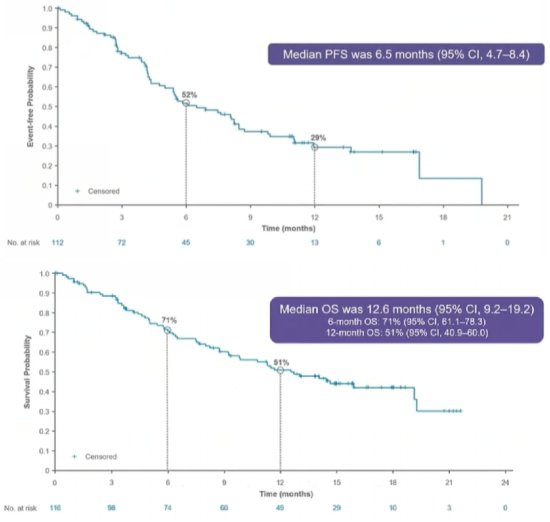
图6. Adagrasib(MRTX849)用于既往接受治疗的KRAS G12C突变NSCLC患者的中位PFS和OS数据[5]
2023年4月,ASCO全体会议上公布了代号为KRYSTAL-1的Ⅱ期研究(NCT03785249)的更新数据,截至2022年10月1日,这项研究共入组了57位KRAS G12C阳性的实体肿瘤患者,包括胰腺癌、胆道系统肿瘤、阑尾癌、卵巢癌等。结果显示:总客观缓解率(ORR)为35.1%,疾病控制率(DCR)高达86.0%,这意味着近90%的患者肿瘤不同程度的缩小或控制稳定;中位随访时间为16.8个月,中位无进展生存期(PFS)为7.4个月;中位总生存期(OS)为14.0个月,6个月、12个月的总生存率分别为84.0%和 53.5%。这意味着超过一半的晚期癌症患者生存时间超过1年。

D-1553产品是益方生物自主研发的一款KRAS G12C抑制剂,拟用于治疗带有KRAS G12C突变的非小细胞肺癌、结直肠癌等多种癌症,是国内首个自主研发并进入临床试验阶段的KRAS G12C抑制剂,也是首个获得CDE突破性治疗品种的国产KRAS G12C抑制剂。D-1553在国际多中心正在进行单药和联合用药在非小细胞肺癌一线治疗以及结直肠癌等其他实体肿瘤中的临床研究,并于2022年5月获得国家药监局药品审评中心(CDE)同意,在中国开展单药治疗KRAS G12C突变阳性非小细胞肺癌患者的单臂II期注册临床试验。该注册临床试验已完成患者入组,目前正在准备NDA申报工作。



图8. 2023 V3 NCCN非小细胞肺癌诊疗指南推荐进行KRAS检测[7]

目前检测KRAS基因突变的方法主要有荧光PCR法、Sanger法、数字PCR法、NGS等。其中Sanger法灵敏度偏低,只能检测到10%~20%以上的突变;NGS法与数字PCR法成本高,操作流程繁琐;而荧光PCR法检测KRAS基因突变,具有灵敏度高,特异性高,且检测便捷快速等优势,目前在临床应用广泛。

图10. 检测流程图
参考文献
[1] Malumbres M, Barbacid M. RAS oncogenes: the first 30 years. Nat. Rev. Cancer.3(6),459–465(2003).
[2] Jonathan M Ostrem, al;K-Ras(G12C) inhibitors allosterically control GTP affinity and effector interactions.Nature 2013 Nov 28;503(7477):548-51.
[3] Salman R. Punekar, Vamsidhar Velcheti, al; The current state of the art and future trends in RAS-targeted cancer therapies.Nature Reviews Clinical Oncology volume 19, pages637–655 (2022).
[4] de Langen AJ, Johnson ML, Mazieres J, et al. Sotorasib versus docetaxel for previously treated non-small-cell lung cancer with KRASG12C mutation: a randomised, open-label, phase 3 trial. Lancet. 2023;401(10378):733-746.
[5] 2022 年美国临床肿瘤学会(ASCO).KRYSTAL-1研究(摘要号:9002).
[6] Pant S, Yaeger R, Spira AI, et al. KRYSTAL-1: activity and safety of adagrasib (MRTX849) in patients with advanced solid tumors harboring a KRAS G12C mutation. J Clin Oncol. 2023; 41(suppl36): 425082.doi: 10.1200 / JCO. 2023. 41. 36_ suppl.425082.
[7] NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®). Non-Small Cell Lung Cancer. Version 3.2023.
[8] CSCO. 非小细胞肺癌临床诊疗指南. 2023版.
[9] Pasi A. Jänne, M.D., Ph.D., et al.Adagrasib in Non–Small-Cell Lung Cancer Harboring a KRAS G12C Mutation. N Engl J Med 2022; 387:120-131.
[10] Reck M, Carbone DP, Garassino M, et al. Targeting KRAS in non-small-cell lung cancer: recent progress and new approaches[J]. Ann Oncol. 2021 Sep;32(9):1101-1110.
[11] The current state of the art and future trends in RAS-targeted cancer therapies. Nat Rev Clin Oncol.2022 Aug 26:1-19.
[12] Yeh J, et al. Remarkable Intracranial Response to Sotorasib in a Patient With KRAS G12C-Mutated Lung Adenocarcinoma and Untreated Brain Metastases: A Case Report. JTO Clin Res Rep. 2022;3(12):100428.
本文标签: 实体肿瘤试剂 检测试剂盒 血液肿瘤试剂 传染病医疗检测试剂
咨询热线
400-007-1121央视《匠心》栏目视角看迈杰转化医学