
肿瘤免疫治疗如火如荼
近年来,肿瘤免疫治疗不断突破创新, 是继手术、化疗、放疗、靶向疗法之后的一个新兴的癌症治疗方式。创新的免疫疗法是癌症患者的希望之星,2013年被《Science》评为年度十大科技突破之首;2018年诺贝尔生理学或医学奖颁给了致力于肿瘤免疫疗法的美国科学家James P. Allison和日本科学家Tasuku Honjo来表彰二人在免疫检查点CTLA-4与PD-1研究方面的贡献 ,截止到2019年2月,FDA已批准43种检查点免疫疗法上市[1]。2018年也是中国免疫治疗的元年, 纳武利尤单抗(O药)和帕博利珠单抗(K药)先后 在国内获批上市,国产特瑞普利单抗和信迪利单抗也不甘落后相继获批,自此开启了国内肿瘤免疫治疗的新时代。 以PD-1/PD-L1单抗为代表的免疫治疗手段在临床上治疗效果越来越好,日渐成为研发和投资热点。

图1. 2018年诺贝尔生理学或医学奖获得者(诺贝尔官网)

图2. 肿瘤免疫治疗发展史[1]
2019年9月, Nature ReviewsDrug Discovery 上发表了一篇综述,介绍了2019年肿瘤免疫疗法的药物研发管线与热门靶点,并与2017年做了对比。结果显示:
①2年的时间,药物研发管线增长了91%,T细胞靶向免疫调节剂开发位居首位[2];
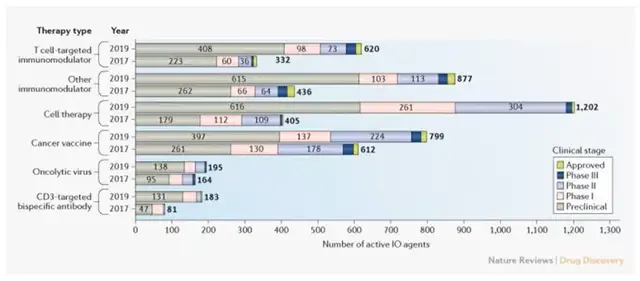
图3. 全球肿瘤免疫治疗研发管线(2017-2019)[2]
②创新靶点增幅78%,PD-1/PD-L1为研究热点,发展势头迅猛[2]。
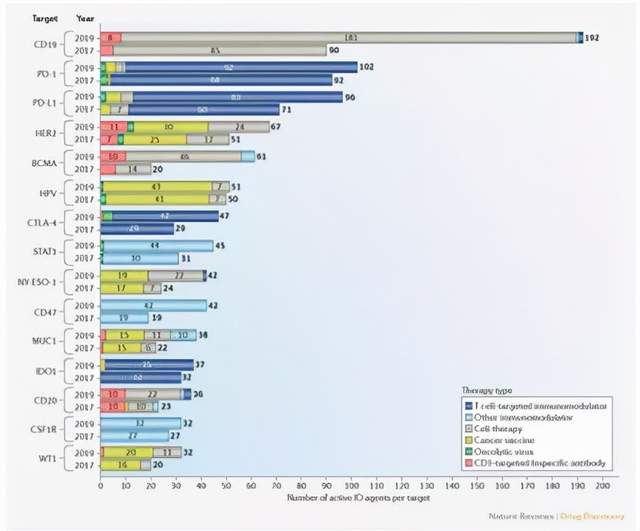
图4. 全球免疫治疗热门靶点Top 15(2017-2019)[2]
PD-1/PD-L1免疫检查点抑制剂作用机理
T细胞活化需要双信号系统调控:信号1是T细胞表面的TCR(T细胞受体)与抗原呈递细胞(APCs)表面的主要组织相容性复合体(MHC)的结合形成抗原肽-MHC复合物,信号2又称为协同共刺激信号,T细胞共刺激表面受体CD28与APCs表面的配体CD80(也称B7-1)或CD86(也称B7-2)结合。一旦激活,T细胞表面就开始表达共抑制性细胞表面受体,如细胞毒性T淋巴细胞抗原4(Cytotoxic T Lymphocyte antigen 4, CTLA4)和程序性细胞死亡蛋白-1(Programmed Cell Death-1, PD-1)。PD-1通常表达于活化的T细胞膜上,其配体为PD-L1(Programmed CellDeath-Ligand 1,程序性细胞死亡蛋白-配体1)。正常情况下,活化的T细胞可以监测并清除肿瘤细胞。然而肿瘤细胞表面的PD-L1可以与T细胞表面的PD-1结合,抑制T细胞活性。免疫检查点抑制剂(Immune Checkpoint Inhibitors, ICIs)可阻断肿瘤细胞PD-L1与T细胞PD-1的结合,解除肿瘤细胞对T细胞的抑制,重新激活免疫系统杀伤癌细胞[3]。
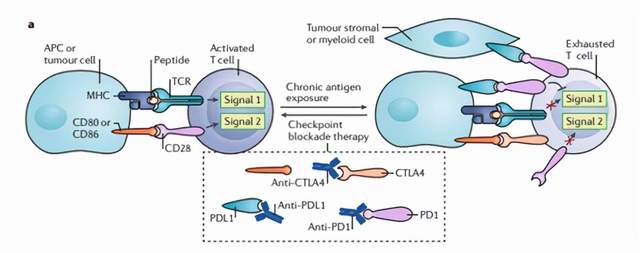
图5. 免疫检查点抑制剂作用原理[3]
国内获批上市的PD-1/PD-L1抑制剂与检测试剂
继2018年第一款PD-1抗体药物—纳武利尤单抗在国内获批之后,截止到目前国内已上市6款进口PD-1抑制剂(进口2款,国产3款),2款进口PD-L1抑制剂[4]:

图6. 国内已上市PD-1/PD-L1抗体药物(数据来源:NMPA官网)[4]
目前与PD-1/PD-L1免疫检查点 抑制剂 配套使用的检测试剂为PD-L1抗体试剂,主流的有4种,分别是来自Dako的22C3、28-8、Ventana的SP263、SP142。其中22C3pharmDX、28-8pharmDX、SP263Assay和SP142Assay获FDA批准上市,22C3pharmDX、28-8pharmDX、SP263Assay获NMPA批准上市。[4-5]
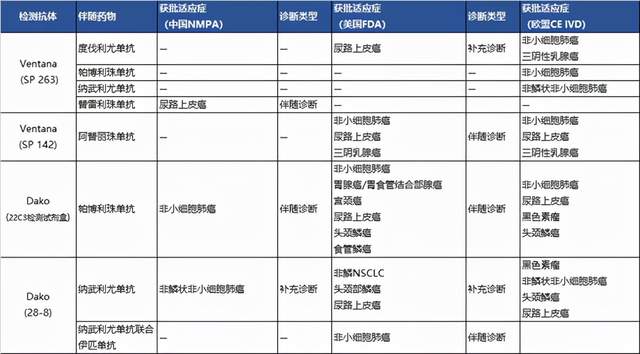
表1. 国内已获批上市的检测抗体(图片来源NMPA、FDA官网)[4-8]
迈杰转化医学PD-L1检测及伴随诊断开发完整解决方案
凭借多组学综合性转化医学平台,迈杰转化医学聚焦生物标志物、伴随诊断,及分子检测与临床用药指导,提供全面的精准诊断方案,服务于创新药企、广大科研机构,PD-L1检测服务与伴随诊断多点布局。
在PD-L1检测服务方面,我们有着雄厚的实力和丰富的经验
迈杰转化医学可为合作伙伴提供市面上所有主流抗体及FDA、NMPA批准的检测试剂的检测服务,包括目前国际国内普遍认可的22C3、28-8、SP263、SP142和我们自主开发的PD-L1检测试剂盒迈普康的抗体MJXXX等克隆号的抗体及配套的LeicaBond Max,VentanaBenchmark,和DakoAutostainer Link48等全自动平台。

图7. 迈杰转化医学病理平台部分仪器展示
①迄今为止,迈杰转化医学已与多家创新药企展开PD-L1免疫组化检测项目的合作,针对以上主流检测抗体,已成功建立基于Leica Bond Max,Ventana Benchmark, 和Dako Autostainer Link48平台的多个癌种的方法学验证。下图为部分完成方法学验证的癌种展示:
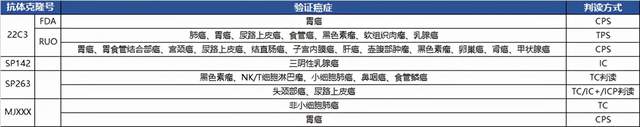
表2. 已完成方法学验证的部分癌种
②迈杰转化医学PD-L1的检测数量多达数万例,涵盖了市面上所有的主流抗体和全自动检测平台,报告和质控精准,检测样本数量和癌种数量在国内首屈一指。
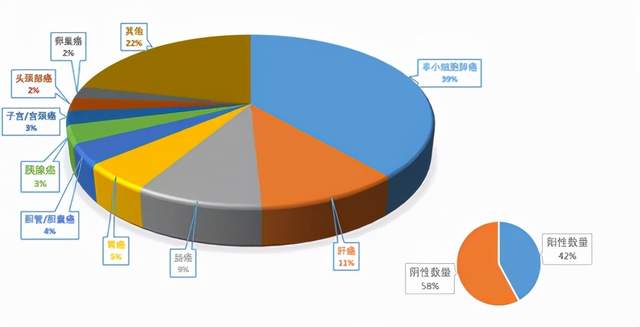
图8. 迈杰转化医学PD-L1检测数量多达数万例,涵盖多种实体瘤(数据截止至4/2020)
① 迈杰转化医学可提供TPS/CPS/TC/IC等多种专业判读方式,所有检测均按照FDA/NMPA批准的cut-off值精准判读。
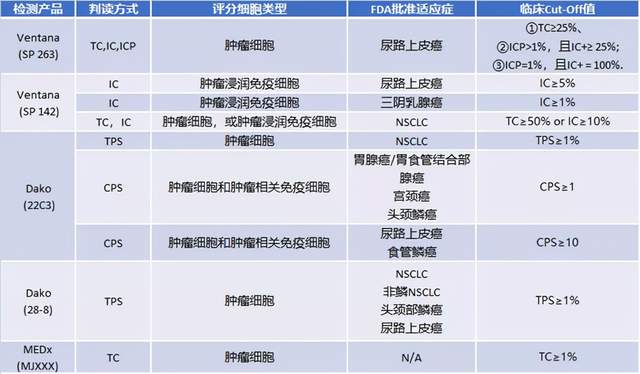
表3. 迈杰转化医学提供专业的判读[4-5]
②拥有高质量的质量管理体系,全部采用原厂试剂,自动化平台,减少人为错误,确保流程稳定和结果一致;严格进行日质控与周质控、阳性与阴性质控的检测;并定期通过美国病理学家协会(CAP)的能力认证,为所有客户提供准确、可靠的检测保证。
依托全平台,可实现一次送样多维度评估免疫指标(PD-L1+TMB+MSI等),更准确预测免疫疗效,最大化囊括免疫检查点抑制剂获益人群。 除此之外,我们还可以检测CD4、CD8水平来评估肿瘤的免疫微环境;提供基于PerkinElmer Vectra 3 System平台的多重免疫组化(mIHC)检测服务,同时检测多个指标,对于肿瘤免疫治疗具有更佳的预测价值。
迈杰转化医学拥有丰富的PD-L1伴随诊断开发和商业化 经验
伴随诊断在新药研发中起到了至关重要的作用,可通过检测特定的生物标记物来预测患者能否从特定药物中获益,对指导临床肿瘤病人用药有重要意义。新肿瘤突变的发现、靶向药研发的加速、医保的覆盖以及新生物标志物的发现,都将驱动伴随诊断市场迅速增长。2014年美国FDA出台了伴随诊断指南,要求某些疾病的治疗药物必须同时有伴随诊断产品才能上市;近日国家药品监督管理局也已启动《伴随诊断试剂与抗肿瘤药物同步研发的临床试验技术指导原则》的编制工作,诊断公司与制药企业合作,共同开发药物和伴随诊断产品势在必行。
迈杰转化医学依托全组学平台专注于药物伴随诊断研发及商业化,已有多款产品上市,多个产品进入临床实验阶段同时还有多个肿瘤新药伴随诊断产品进入研发管线,涵盖靶向治疗、免疫治疗和细胞治疗。已与多家创新药企建立战略合作关系,合作开发伴随诊断。
迈杰转化医学已经与多家创新药企建立战略合作关系,共同开发PD-L1 伴随诊断试剂盒,助力精准诊断。同时自主研发了基于Lecia Bond MAX平台的PD-L1抗体检测试剂(商品名:迈普康),用来评估肿瘤细胞中PD-L1蛋白的表达水平,有望成为国内首家获批的PD-L1检测试剂盒。

图9. 在TC≥50%级别下,迈普康能检测更高表达比例的肿瘤细胞
发起中国版“Blueprint计划”
作为精准诊断行业整体解决方案的开拓创新者和领导者,迈杰转化医学与中国生物工程学会精准医疗与伴随诊断专业委员会共同发起和组织了中国版Blueprint项目,旨在发现免疫治疗受益人群,提高PD-L1检测方法的一致性,推动PD-L1检测剂本土化,尽快形成专家共识及行业规范,为中国生物医药的创新发展、为中国诊断产品的国产化加快步伐、为中国及所有的患者获益而共同努力。
近期,迈杰转化医学就即将上市PD-L1检测试剂盒—迈普康与市面上普遍认可的3种抗体在非小细胞肺癌和胃癌样本的一致性进行了对比研究:
①迈普康、SP263和22C3在19例非小细胞肺癌(NSCLC)样本的一致性分析比较:
共收集了19例非小细胞肺癌(NSCLC)组织样本,PD-L1的表达判读采用TC评分,只计算肿瘤细胞染色百分比。结果显示:迈普康、22C3检测肿瘤细胞PD-L1表达具有较高的一致性,均高于SP263的灵敏度。下图展示为同一样本切片,用3种不同的抗体,染色情况。
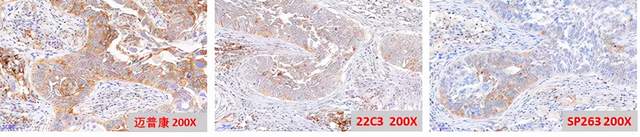
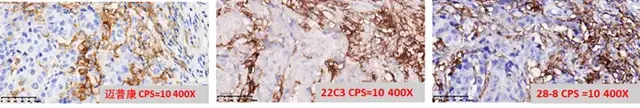
②迈普康、22C3和28-8在50例胃癌(GC)样本的一致性分析比较:
共收集了50例胃癌组织样本,由3名病理医生参与PD-L1免疫组化的判读。PD-L1的表达判读参考22C3,判读CPS,评估肿瘤细胞和肿瘤相关免疫细胞。结果显示:3款PD-L1抗体对肿瘤细胞和肿瘤相关免疫细胞均有不同程度的染色。迈普康、 22C3检测结果具有较高的一致性,且不低于95%。而28-8的灵敏度偏低。
依托行业领先的核酸、蛋白、病理以及细胞生物学等综合性转化医学平台和经验丰富的专业化技术团队,我们已为广大药企客户临床研究及临检客户、生物公司及 科研客户提供了大量准确而高效的PD-L1伴随诊断开发与检测服务,已赢得了广大客户和合作伙伴的赞誉和信赖。我们将一如既往地提供转化医学服务解决药物研发痛点,提供伴随诊断开发解决患者用药痛点。不忘初心,方得始终,希望继续得到您的关心和支持!
参考文献
[1] Jérôme Galon,Daniela Bruni. Tumor Immunologyand Tumor Evolution: Intertwined Histories. Immunity Review. doi:10.1016/j.immuni.2019.12.018.
[2] Yu et al., (2019). Immuno-oncology drug developmentgoes global. Nature Reviews Drug Discovery. doi: 10.1038/d41573-019-00167-9.
[3] Havel, J.J., Chowell, D. & Chan, T.A. Theevolving landscape of biomarkers for checkpoint inhibitorimmunotherapy. Nat Rev Cancer19, 133–150 (2019). doi:10.1038/s41568-019-0116-x
[4] http://app1.nmpa.gov.cn/datasearchcnda/face3/base.jsp?tableId=26&tableName=TABLE26&title=%B9%FA%B2%FA%C6%F7%D0%B5&bcId=118103058617027083838706701567
[5] https://www.fda.gov/medical-devices/vitro-diagnostics/list-cleared-or-approved-companion-diagnostic-devices-vitro-and-imaging-tools
[6]diagnostics.roche.com/global/en/products/tests/ventana-pd-l1-_sp263-assay2.html
[7] https://diagnostics.roche.com/global/en/products/tests/ventana-pd-l1-_sp142-assay2.html#productSpecs
[8] https://www.agilent.com/search/?Ntt=PD-L1%20IHC%2028-8%20pharmDx%20Diagnostic%20in%20Europe&redirect=0
原创:Grace
编辑:Grace